Parcerias institucionais estratégicas com empresas que vivem o universo das Análises Clínicas. Veja nosso portfólio institucional de divulgação.
Diluição de soluções no laboratório: cálculo, exemplos e como fazer corretamente
Aprenda como fazer diluição de soluções no laboratório usando o cálculo C1V1 = C2V2, exemplos práticos e erros comuns. Inclui calculadora gratuita para preparar soluções com precisão.
COLETA E PREPARO
Ariéu Azevedo Moraes
3/16/20264 min ler


Diluição de soluções no laboratório: o cálculo que sustenta quase todos os exames
Diluição de soluções é o processo de reduzir a concentração de uma substância adicionando solvente sem alterar a quantidade de soluto presente. No laboratório, esse cálculo permite preparar reagentes, padrões e amostras em concentrações específicas, geralmente usando a relação C1V1 = C2V2, que conecta concentração e volume antes e depois da diluição.
Por que a diluição é um cálculo fundamental no laboratório
Existem cálculos complexos em análises clínicas: anion gap, clearance de creatinina, HOMA-IR, índices hematimétricos. Mas poucos são tão universais no laboratório quanto a diluição de soluções. Ela aparece em praticamente todas as áreas:
bioquímica clínica
microbiologia
hematologia
imunologia
biologia molecular
Sempre que um reagente concentrado precisa ser ajustado para uma concentração específica, a diluição entra em cena.
É um dos primeiros cálculos que um estudante aprende e um dos que mais se usa na prática.
O que significa diluir uma solução
Diluir uma solução significa reduzir sua concentração adicionando solvente, mantendo a quantidade de soluto constante. Isso significa que o que muda é o volume total da solução, não a quantidade da substância dissolvida.
Imagine uma solução concentrada de sal dissolvida em água. Se você adicionar mais água sem alterar a quantidade de sal, a solução ficará mais diluída. No laboratório, esse princípio permite preparar concentrações específicas necessárias para testes e reações químicas.
O cálculo clássico de diluição
A relação mais utilizada para calcular diluições conecta concentração e volume antes e depois do preparo da solução. Ela diz que:
Concentração inicial multiplicada pelo volume inicial é igual à concentração final multiplicada pelo volume final.
Em forma simplificada:
C1 × V1 = C2 × V2
Onde:
C1 representa a concentração inicial
V1 representa o volume da solução concentrada utilizado
C2 representa a concentração desejada
V2 representa o volume final da solução após diluição
Essa relação funciona porque a quantidade de soluto permanece constante antes e depois da diluição.
Exemplo prático de diluição no laboratório
Imagine que um laboratório possui uma solução estoque de um reagente com concentração de 100 mg/mL.
O protocolo exige uma solução de 10 mg/mL com volume final de 10 mL.
Aplicando o raciocínio da diluição, descobre-se quanto da solução concentrada deve ser utilizado e quanto solvente deve ser adicionado. Esse tipo de cálculo é rotina na preparação de:
reagentes
padrões de calibração
controles laboratoriais
diluições de amostras biológicas
Diluição em análises clínicas
Na rotina de um laboratório clínico, diluições aparecem em diversos contextos:
Diluição de amostras: Quando um analito está muito alto para o equipamento, a amostra pode ser diluída para permitir leitura adequada.
Preparação de reagentes: Muitos kits laboratoriais exigem diluição de reagentes concentrados.
Curvas de calibração: Ensaios imunológicos e bioquímicos utilizam séries de diluições para gerar padrões.
Microbiologia: Diluições seriadas são utilizadas para contagem bacteriana ou viral.
Por isso, dominar esse cálculo reduz erros pré-analíticos e melhora a confiabilidade dos resultados.
Diluições seriadas: quando uma não basta
Em muitos testes laboratoriais, uma única diluição não é suficiente.
Nesses casos, realizam-se diluições seriadas, nas quais cada solução preparada se torna a base para a próxima.
Esse método é comum em:
titulações
microbiologia
testes imunológicos
biologia molecular
Ele permite atingir concentrações muito baixas de forma controlada e reproduzível.
Erros comuns em diluições laboratoriais
Mesmo sendo um cálculo simples, alguns erros aparecem com frequência:
Unidades incompatíveis: Volumes ou concentrações devem estar na mesma unidade.
Erro de pipetagem: Micropipetas mal calibradas alteram o resultado final.
Confusão entre volume final e volume adicionado: O cálculo sempre se refere ao volume final da solução, não apenas ao solvente adicionado.
Erro na diluição seriada: Pequenos erros acumulados podem gerar diferenças grandes no resultado final.
Por isso, padronização e ferramentas de cálculo ajudam muito na rotina.
Calcule diluições rapidamente com a PipetaCalc
Para evitar erros manuais e agilizar o preparo de soluções no laboratório, desenvolvemos uma ferramenta específica.
Calculadora de diluição de soluções – PipetaCalc
Ela permite calcular rapidamente:
volume da solução estoque
volume final desejado
concentração final da solução
Ideal para estudantes, profissionais de laboratório e pesquisadores.
Concluímos
A diluição de soluções é um dos cálculos mais básicos, e ao mesmo tempo mais importantes, da rotina laboratorial. Ela conecta matemática simples com precisão experimental, permitindo preparar reagentes, calibrar equipamentos e ajustar concentrações de forma confiável.
Dominar esse cálculo não é apenas um exercício acadêmico.
É uma habilidade prática que sustenta a qualidade de inúmeros exames e experimentos científicos.
Ariéu Azevedo Moraes
Biomédico | Especialista em Gestão laboratorial
Fundador da Pipeta e Pesquisa
🔬 Descomplicando as análises clínicas com interpretação e prática aplicada
Referências
LibreTexts Chemistry. Dilutions and concentrations. Disponível em: https://chem.libretexts.org/Courses/Valley_City_State_University/Chem_121/Chapter_4%3A_Solution_Chemistry/4.5%3A_Molarity_and_Dilutions (Chemistry LibreTexts)
TopTipBio. The C1V1 = C2V2 equation explained. Disponível em: https://toptipbio.com/c1v1-equation/ (Top Tip Bio)
Byju's Learning. Dilution formula and examples. Disponível em: https://byjus.com/dilution-formula/ (BYJU'S)
Deixe seu comentário









Confira nosso Canal!

Confira esses títulos abaixo:
Descubra por que alguns exames laboratoriais demoram mais para ficar prontos, como funciona o processo dentro do laboratório e quais fatores influenciam o tempo de liberação dos resultados.
Descubra como alimentos como ovos, chocolate, soja, glúten, chia e manteiga podem influenciar exames laboratoriais e o que a bioquímica clínica revela sobre essa relação.
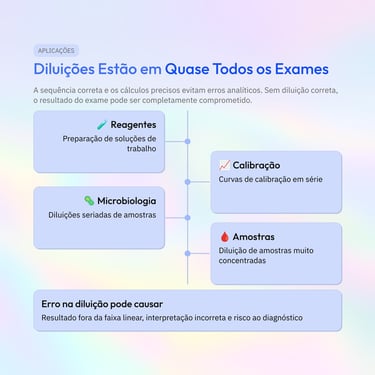
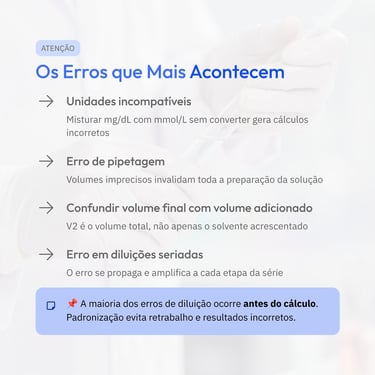
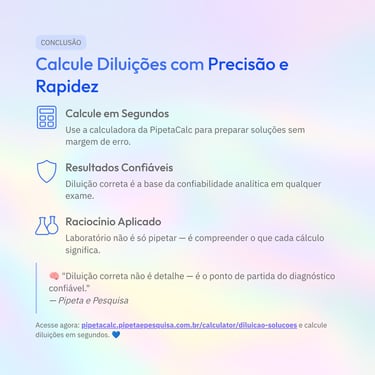
Leitura rápida: principais pontos deste artigo
Para quem prefere uma visualização direta, os cards resumem os conceitos centrais abordados ao longo do texto, facilitando a revisão e a compreensão rápida dos temas discutidos.
Informações sobre saúde e Análises Clínicas para todos.
© 2025. Todos o Direitos Reservados - Pipeta e Pesquisa
BRASIL
TRÊS LAGOAS - MS
79600-000
Agendar Exames
Instrumental Laboratorial
Logística Laboratorial
"A Pipeta e Pesquisa opera através de suas unidades estratégicas: Pipeta Store, especializada em suprimentos; Pipeta Tech, focada em inovação laboratorial; e o Blog da Pipeta e Pesquisa, nosso hub de inteligência e educação."
